Zespół łamliwego chromosomu X to najczęstsza rodzinna przyczyna niepełnosprawności intelektualnej, jak również najczęstsza jednogenowa przyczyna autyzmu. Występuje z częstością 1 na 4000–6000 żywych noworodków męskich. Ze względu na dziedziczenie sprzężone z chromosomem X rzadziej pojawia się u dziewczynek. Zaburzenia zachowania w zespole to np. problemy z mową, labilność emocjonalna, cechy autystyczne, stereotypie ruchowe.
Zespół łamliwego chromosomu X
Podstawy molekularne i dziedziczenie zespołu Martina–Bella
Zespół FRAX (zespół łamliwego chromosomu X, zespół Martina-Bella, ang. fragile X syndrome) jest związany z mutacją w genie FMR1 (ang. fragile X mental retardation 1), w tzw. "miejscu łamliwym" chromosomu X – Xq27.3. Dziedziczy się jako zespół dominujący sprzężony z chromosomem X – mężczyźni z pełną mutacją, jako że posiadają tylko jeden chromosom X, mają pełne objawy choroby. Kobiety, nawet dotknięte pełną mutacją, ze względu na to, że mają dwa chromosomy X, wykazują łagodniejsze objawy choroby, bo w każdej komórce jeden z nich ulega inaktywacji.
Jest to pierwszy opisany zespół chorobowy z grupy mutacji dynamicznych, inne przykłady to:
- pląsawica Huntingtona,
- ataksja Friedreicha.
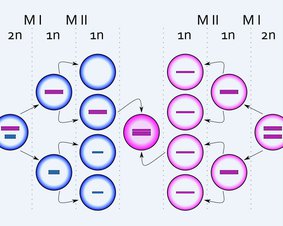
Mutacje dynamiczne polegają na powieleniu fragmentu genu – zazwyczaj długości 3 nukleotydów (składowych kodu genetycznego). W przypadku zespołu łamliwego chromosomu X dochodzi do wielokrotnego powielenia trójnukleotydu CGG w nieulegającym translacji ("przepisaniu" na białko) odcinku 5’ genu FMR1. Zakres powtórzeń CGG u zdrowych osób wynosi 5–58. Allele (pojedyncze kopie genu), które posiadają 40 lub mniej powtórzeń, są przekazywane potomstwu w sposób stabilny – liczba powtórzeń nie wzrasta po mejozie (specjalnym podziale komórek płciowych, zachodzącym w jądrach i jajnikach). Allele, które zawierają 41–58 powtórzeń są niestabilne – podczas mejozy ilość kopii CGG może się powiększyć, co może wywołać premutację u potomstwa. Z kolei premutacja (59–200 powtórzeń) może w kolejnym pokoleniu awansować do pełnej mutacji (ponad 200 kopii, najczęściej od kilkuset do kilku tysięcy), która jest powiązana z metylacją promotora genu FMR1, zahamowaniem transkrypcji ("przepisywania" DNA na RNA), a w konsekwencji brakiem białka.
Przeczytaj też: Tiki nerwowe – przyczyny, objawy, leczenie
Białko powstające w wyniku translacji genu FMR1 odgrywa bardzo ważną rolę w funkcji synaps (połączeń między komórkami nerwowymi), a szczególnie ich dojrzewaniu i eliminacji. Białko to w normalnych warunkach obecne jest w dużej ilości oczywiście w mózgu, a także w jądrach. Jego brak jest przyczyną objawów zespołu łamliwego chromosomu X, ale w pewnych analizach stwierdzono jego ubytki również u pacjentów z:
- chorobą afektywną dwubiegunową (60%),
- poważną depresją (68%),
- schizofrenią (78%).
Obraz kliniczny zespołu łamliwego chromosomu X
Zespół łamliwego chromosomu X może występować u obu płci i mieć szeroki wachlarz objawów klinicznych, które są bardziej nasilone u mężczyzn. U chłopców po okresie dojrzewania głównie obserwuje się niepełnosprawność intelektualną (od umiarkowanej do znacznego stopnia), której towarzyszy szereg zaburzeń behawioralnych. Chorzy wykazują specyficzne dysfunkcje intelektualne, w tym osłabienie:
- uwagi i funkcji wykonawczej,
- pamięci krótkoterminowej i wzrokowej,
- koordynacji wzrokowo-przestrzennej i postrzegania,
- planowania i analizy bodźców arytmetycznych.
Chorzy mają przy tym dobrą wiedzę ogólną i umiejętności pozwalające na radzenie sobie w codziennym życiu. U dzieci występuje opóźnienie rozwoju psychoruchowego i silnie opóźniony rozwój mowy, któremu towarzyszą zaburzenia zachowania.
Zaburzenia zachowania, jakie mogą pojawiać się w zespole łamliwego chromosomu X to:
- zaburzenia koncentracji uwagi,
- labilność emocjonalna,
- zaburzenia adaptacji,
- cechy autystyczne (kryteria autyzmu są spełniane przez 25–35% chorych),
- stereotypie ruchowe (klaskanie, machanie rękami),
- nadmierna ruchliwość,
- problemy z mową,
- echolalia (powtarzanie słów/zwrotów wypowiedzianych przez inne osoby),
- agresja i autoagresja,
- nadwrażliwość na bodźce dotykowe,
- unikanie kontaktu wzrokowego,
- napady złości,
- depresja i stany lękowe.
Inne objawy kliniczne w zespole łamliwego chromosomu X to powiększenie jąder po okresie pokwitania (są one 2–3 razy większe niż u zdrowych rówieśników) oraz symptomy związane z dysplazją tkanki łącznej:
- wydłużona, wąska twarz,
- powiększone, odstające małżowiny uszne (jest to najbardziej stały objaw u dzieci z zespołem łamliwego chromosomu X, u których reszta cech jest jeszcze słabo wyrażona; występuje u 80% osób dotkniętych tym zespołem),
- płaskostopie,
- wypadanie płatka zastawki mitralnej,
- nadmierna ruchomość stawów międzypaliczkowych rąk,
- delikatna, miękka skóra.
Kobiety – nosicielki pełnej mutacji mają lżejsze objawy. U 50% z nich może występować upośledzenie intelektualne lekkiego stopnia lub problemy w nauce, zaburzenia emocjonalne, lęk i niepokój oraz depresja. Nadmierna nieśmiałość może być u nich jedynym objawem. Nieprawidłowości wyglądu są subtelne – delikatnie wydłużona twarz i powiększone małżowiny uszne.
Kobiety obarczone jedynie premutacją zwykle wykazują normalny rozwój intelektualny, ale mogą wykazywać obniżenie nastroju, niską samoocenę. Około 40 roku życia może pojawić się u nich przedwczesna menopauza (16–20% przypadków) lub mogę mieć problemy z zajściem w ciążę.
U mniej niż 10% osób z zespołem łamliwego chromosomu X opisano cechy, takie jak:
- otyłość,
- hiperfagia (nadmierne łaknienie),
- hipogonadyzm,
- opóźnienie dojrzewania.
Zespół łamliwego chromosomu X a zespół Pradera-Williego
Częściej u tych osób zauważane były cechy autystyczne. Taki obraz kliniczny nazwano fenotypem Pradera-Williego (ang. Prader-Willi phenotype, PWP), gdyż podobne cechy są obecne w zespole Pradera-Williego (ang. Prader-Willi syndrome, PWS). W przeciwieństwie do PWS, dzieci z zespołem łamliwego chromosomu X i PWP nie mają hipotonii mięśni i wynikających z niej problemów z przyjmowaniem pokarmów w dzieciństwie, a początek hiperfagii następuje dopiero około 5 roku życia.
Kolejna cecha różnicująca to fakt, iż dzieci z PWP zupełnie nie kontrolują ilości spożywanych pokarmów, co prowadzi u nich do wymiotów, za to dzieci z PWS raczej nie wymiotują. Różnicujące są również badania genetyczne – dzieci z PWP mają stwierdzone zaburzenia ekspresji genu CYFIP1 (lokalizacja 15q11-q13), przez co powstaje mniej białka, które w prawidłowych warunkach współpracuje z produktem genu FMR1. Dzieci z PWS z kolei mają stwierdzoną albo delecję regionu 15q11-q13 w allelu ojcowskim, albo uniparentalną disomię chromosomu 15 ze strony matki.
Zespół drżenia i ataksji związany z łamliwym chromosomem X
U mężczyzn powyżej 50 roku życia – nosicieli premutacji opisano chorobę neurodegeneracyjną – zespół drżenia i ataksji związany z łamliwym chromosomem X. Występują u nich objawy sugerujące upośledzenie funkcji móżdżku: postępujące drżenie zamiarowe (drżenie w końcowej części ruchu, np. wyciągania ręki po przedmiot) i niezborność móżdżkowa, którą można zauważyć obserwując chód pacjenta – jest to tzw. marynarski chód, na szerokiej podstawie, który może być zaburzony przez upadki. W chorobie tej obecny jest również parkinsonizm i otępienie. Za główne kryterium rozpoznania tej jednostki chorobowej uznano charakterystyczny obraz rezonansu magnetycznego mózgu, na który składają się:
- symetryczne wzmożenie intensywności sygnałów w projekcji T2 w istocie białej oraz środkowym konarze móżdżku,
- uogólniony zanik mózgu z poszerzeniem komór mózgu.
Zespół łamliwego chromosomu X u dzieci
U małych dzieci z zespołem łamliwego chromosomu X częste są (prawdopodobnie ze względu na dysplazję tkanki łącznej) infekcje ucha środkowego, rzadziej zatok obocznych nosa. Takie zakażenia muszą być intensywnie leczone, aby nie wprowadzać dalszych utrudnień dla rozwoju mowy. Rzadziej występują:
- bezdechy,
- tiki,
- refluks żołądkowo-przełykowy (może prowadzić do nawracających wymiotów i zaburzeń masy ciała),
- przepukliny,
- przemieszczenia stawów,
- kłopoty z narządem wzroku (zez, oczopląs, wady refrakcji),
- padaczka.
Napady padaczki zdarzają się częściej u chłopców niż u dziewczynek z zespołem łamliwego chromosomu X. Są to najczęściej napady uogólnione lub częściowe złożone, które mają tendencję do ustępowania w późniejszym dzieciństwie i dorosłości. Najczęściej udaje się je opanować za pomocą jednego leku, ale przy jego wyborze należy uważać na objawy uboczne (szczególnie na nasilenie hipotonii, niezgrabności i pogorszenie funkcji poznawczych). Większość pacjentów najlepiej reaguje na karbamazepinę i kwas walproinowy, a lamotrygina, okskarbamazepina, zonisamid i lewetiracetam są efektywne w skojarzonej terapii trudnych do wyciszenia napadów. Trzeba unikać gabapentyny i fenobarbitalu (z powodu pogarszania zaburzeń behawioralnych) oraz fenytoiny (powoduje przerost dziąseł i innych tkanek). Przy podawaniu leków przeciwpadaczkowych trzeba monitorować funkcję wątroby, ogólny stan zdrowia i parametry krwi obwodowej.
Leczenie zespołu łamliwego chromosomu X
Pacjentom z zespołem łamliwego chromosomu X najczęściej podaje się leki przeciwdepresyjne i stymulujące (np. metylfenidat, lek stymulujący, który może zmniejszyć nadruchliwość, zaburzenia koncentracji, napady złości, agresję).
Agoniści receptora adrenergicznego (np. guanfacyna, klonidyna) pomagają kontrolować impulsywność, agresję i nadruchliwość, a inhibitory zwrotnego wychwytu serotoniny (np. fluoksetyna) pomagają zmniejszyć lęk, drażliwość, impulsywność, depresję, zaburzenia nastroju, zachowania kompulsywne, zachowania autoagresyjne.
Leki antypsychotyczne mogą być użyte do kontroli zaburzeń psychotycznych i zachowań agresywnych. Nietypowe leki przeciwpsychotyczne są wykorzystywane w leczeniu autyzmu i zachowań autoagresywnych. W przeszłości najczęściej był stosowany rysperydon (znacznie zmniejszał agresję u starszych pacjentów oraz uporczywe zachowania u mniejszych chłopców, a również zachowania autystyczne). Drugi najczęściej obecnie stosowany atypowy lek przeciwpsychotyczny to aripiprazol – ma wysoką skuteczność (71%) i w najmniejszym stopniu wpływa na przyrost masy ciała. Działania niepożądane tych leków to m.in. zaparcia, cukrzyca, nudności, zwiększenie masy ciała i sedacja (nadmierne uspokojenie).

Hanna Cholewa
Lekarz
Absolwentka Wydziału Lekarskiego w Katowicach (Śląski Uniwersytet Medyczny w Katowicach), obecnie w trakcie odbywania stażu podyplomowego. Uczestniczka zagranicznych praktyk zawodowych z zakresu chirurgii oraz ginekologii i położnictwa, m.in. w Meksyku, Hiszpanii i Niemczech. Zainteresowana nauką języków, podróżami oraz kinem.




 342
342







Komentarze i opinie (0)